AVAC 高通量多重单分子免疫检测分析仪
AVAC高通量多重单分子免疫检测分析仪
-----实验室、生命科学和研发的先进研究工具
原理:
首先生物标志物检测由表面锚定抗体识别,然后由溶液中的抗体识别捕获的自由区域的生物标志物,进而作用在等离子体标记的金纳米粒子上,之后来自纳米粒子的微弱等离子体信号被多介电底物放大。然后分析每个纳米粒子的散射光谱、表征、分类并最终对粒子进行计数。不同纳米粒子参数(例如亮度,光谱信息或偏振态)的组合允许很高的特异性,并且检测范围非常低,可达飞克范围,同时,通过使用不同大小和形状的纳米颗粒,可以同时检测同一样品中的不同生物标志物,达到多重检测的功能。

特点:
1.超灵敏
AVAC其专有的检测技术的灵敏度比ELISA技术高出一百万倍,而ELIS A技术已经成为40多年来蛋白质检测的标准。 这种创新的AVAC技术为需要超灵敏检测的诊断情况提供了解决方案; 此外,该技术也适用于即时医疗(POCT)应用。
2.通用性
AVAC含有一种一次性试剂盒,它由大小为 120x80 mm2 的多介质基板和可拆卸的 96 孔硅胶结构组成。 滤芯的尺寸设计与医院和分析实验室中常规使用的样品处理系统兼容。 最近,又新推出一种具有 16 孔玻片格式的新测试盒。
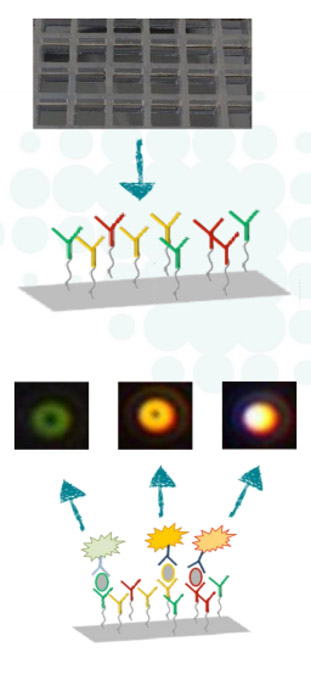
3.光学读取器和粒子计数器功能
通过使用专有的暗场显微分光光度法测量弱散射信号,以光学方式检测等离子体纳米粒子。
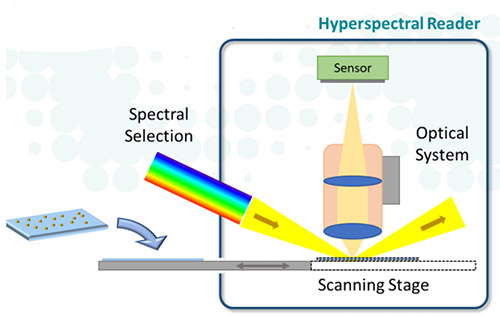
4.单粒子数字计数功能
由于每个等离子体纳米颗粒都与感兴趣的生物标志物特异性结合,因此通过对不同的纳米颗粒进行分类和计数,可以量化固定在基材上的每种生物标志物的数量。
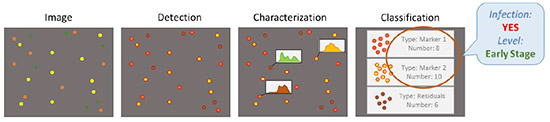
应用(已验证标志物):
-
肿瘤学:
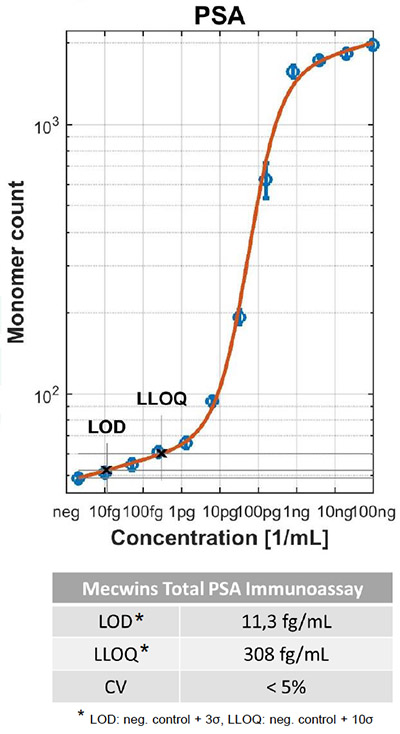
– PSA,前列腺生物标志物,癌症复发检测
– CYFRA21-1 -
心脏疾病:
– 肌钙蛋白 I,心肌梗塞生, 物标志物
-
传染性疾病:
– p24,HIV 生物标志物检测
– 白介素生物标志物(IL-10、IL-6、TNF-α、INF-γ)
– PCT,败血症的生物标志物检测
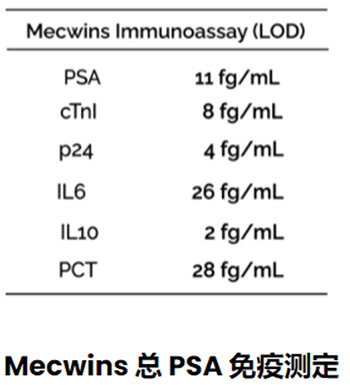
技术参数:
| 空间分辨率 | 读取/分析速度 | 吞吐量 | 多重检测能力 | 用户界面 |
| 0.7 µm(衍射受限) | 每小时最多 20000 张图像 | 在不到 5 分钟的时间内完成 96 个样品 | 多达 5 个生物标志物 | 用于所有输入和输出的集成 15 英寸触摸屏 |


 扫码咨询光刻胶、模板
扫码咨询光刻胶、模板
 扫码咨询红外测温仪、单晶、靶材
扫码咨询红外测温仪、单晶、靶材
 扫码咨询介电阻抗谱、杨氏模量无损测量
扫码咨询介电阻抗谱、杨氏模量无损测量